13.11.2017 Live und in Farbe: Gerüstbauer helfen bei der Kernteilung
Wissenschaftler entdecken das fädige Gerüstprotein F-Aktin nach der Zellteilung in wachsenden Kernen
Lebende Zellen benutzen zum Innenausbau dasselbe Material, das sie auch für die Außenhülle verwenden – so lässt sich zusammenfassen, was Wissenschaftlerinnen und Wissenschaftler um den Marburger Pharmakologen Professor Dr. Robert Grosse herausgefunden haben, als sie die Kernteilung von Zellen beobachteten: Das präzise Wachstum der neuen Zellkerne findet nur statt, wenn sich das Gerüstprotein Aktin darin zu Fäden zusammenlagert, wie man sie bislang nur von der Zellmembran kennt. Das internationale Forschungsteam berichtet über seine Ergebnisse in der aktuellen Ausgabe der Fachzeitschrift „Nature Cell Biology“.
„Wir haben einen Bestandteil des Zellgerüsts gefunden, der den Kern von Säugerzellen reorganisiert, unmittelbar nachdem die Kernteilung stattgefunden hat“, legt Studienleiter Robert Grosse von der Philipps-Universität dar. Ehe eine Zelle sich teilt, muss der Inhalt des Kerns mit den Erbinformationen auf die beiden Hälften der Zelle verteilt werden, die später zu den Tochterzellen werden. Bei der Kernteilung oder Mitose verdichten und verkürzen sich zunächst die Chromosomen, so dass sie leichter zu den gegenüberliegenden Polen der Zelle transportiert werden können.
Die Mitose endet, wenn sich die beiden Tochterzellen voneinander getrennt haben; diese organisieren ihre Zellkerne dann neu, wobei sich die Kerne innerhalb kurzer Zeit stark vergrößern. Diese Reorganisation ist für jede Zellfunktion essentiell; in Krebszellen ist sie häufig gestört.
„Ob Aktinfäden an der Wiederherstellung der Kernarchitektur beteiligt sind, ist bislang nicht untersucht worden“, erklärt Grosses Mitarbeiter Dr. Christian Baarlink, einer der Erstautoren der Studie. Das Gerüstprotein Aktin prägt in Form langer Fäden die Gestalt der Zellaußenhülle und die Zellpolarität, aber auch die Wechselwirkung von Zellen untereinander sowie mit ihrer Umgebung.
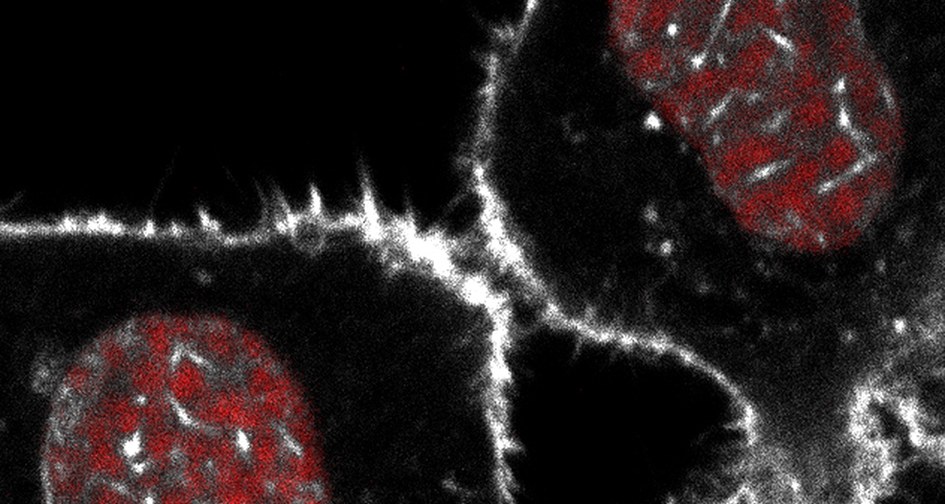
Die Wissenschaftlerinnen und Wissenschaftler beobachteten lebende Zellen während der Kernteilung. Dabei stellten sie durch Färbeexperimente fest, dass sich Aktinfäden bilden, wenn die Tochter-Zellkerne entstehen. Die Fäden messen wenige Mikrometer in der Länge – das entspricht etwa einem Hundertstel der Dicke eines menschlichen Haars. 96 Prozent aller untersuchten Zellen wiesen Proteinfäden in den neu gebildeten Kernen auf, so genanntes F-Aktin.
Die Forschungsgruppe setzte verschiedene pharmakologische Mittel ein, um die Fadenbildung zu unterdrücken und zu ermitteln, wie sich dies auf die Wiederherstellung der Tochterzellkerne auswirkt. „Die Substanzen wurden den Zellen direkt unter dem Mikroskop zugesetzt, wenn diese die Kernteilung beendeten“, erläutert Matthias Plessner, der sich die Erstautorenschaft mit Baarlink teilt.
Das Resultat der Experimente: Setzt man Agentien ein, die verhindern, dass sich Aktin zu Fäden verknüpft, so unterbleibt regelmäßig die Ausdehnung des neugebildeten Kerns.
„Unsere Befunde zeigen, wie wichtig F-Aktin für die Organisation des Zellkerns ist“, betonen die Autoren – „mit allen Folgerungen, die sich daraus für die Stabilität des Erbguts und somit für die menschliche Gesundheit ergeben.“
Robert Grosse leitet das Pharmakologische Institut am Fachbereich Medizin der Philipps-Universität. Neben Grosses Arbeitsgruppe beteiligten sich Wissenschaftlerinnen und Wissenschaftler aus Großbritannien und Japan an den zugrunde liegenden Forschungsarbeiten. Das „Human frontier science program“, die Deutsche Forschungsgemeinschaft und die Wilhelm-Sander-Stiftung sowie weitere Förderer unterstützten die Studie finanziell.

Der Marburger Pharmakologe Professor Dr. Robert Grosse (rechts) sowie (von links) Dr. Stefan Baumeister, Dr. Ulrike Endesfelder, David Virant, Dr. Christian Baarlink und Matthias Plessner aus seiner Arbeitsgruppe erforschen, wie das Gerüstprotein F-Aktin die Kernteilung beeinflusst. (Foto: Jessica Moussi)
Originalveröffentlichung: Christian Baarlink, Matthias Plessner, Alice Sherrard & al.: A transient pool of nuclear F-actin at mitotic exit controls chromatin organization, Nature Cell Biol. 2017, DOI: 10.1038/ncb3641
Kontakt
Professor Dr. Robert Grosse
Tel.: 06421 28-65001 und -65001 (Sekretariat)