Hauptinhalt
Epitheliale Tumoren
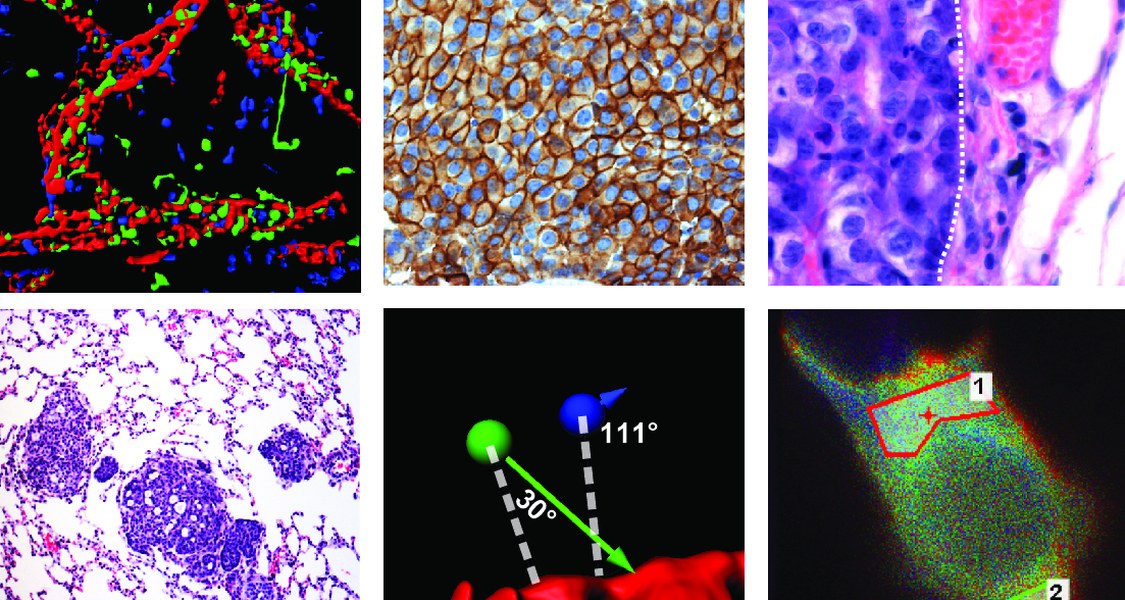
Ein wesentlicher Teil unserer Forschungstätigkeit beschäftigt sich mit der Rolle von Plexinen bei Tumorerkrankungen. So konnten wir zeigen, dass Plexin-B1 mit der onkogenen Rezeptortyrosinkinase ErbB-2 interagiert, und dass diese Interaktion von großer Bedeutung für die Progression ErbB-2-überexprimierender Mammakarzinome ist. Plexin-B1 ist in Mammakarzinomzellen exprimiert, und wird durch überexprimiertes Erb-2- phosphoryliert und aktiviert. Diese Phosphorylierung und Aktivierung von Plexin-B1 und ErbB-2 führt zur Aktivierung der pro-invasiven kleinen GTPasen RhoA und RhoC. Dies fördert die invasivität von Tumorzellen in vitro und ist entscheidend für ihre Metastasierung in vivo. Auch in Tumorbiopsien von Mammakarzinom-Patientinnen konnte eine ErbB-2-abhängige Phosphorylierung von Plexin-B1 nachgewiesen werden. Eine systematische Analyse von humanen microarray-Daten zeigte zudem eine Korrelation von hohen Plexin-B1-Expressionsleveln im Tumorgewebe mit einer schlechten Prognose der Patientinnen. Neu generierte anti-Plexin-B1-Antikörper, die die Interaktion von Plexin-B1 mit ErbB-2 blockieren, hmemen in vitro die Invasivität ErbB-2-überexprimierender Mamma- und Ovarialkarzinomzelllinien.
Eine zusätzliche Ebene in der Komplexität des Semaphorin-Plexin-Systems könnte darin bestehen, dass das System nicht nur uni- sondern auch bidirektionale Signaltransduktion vermitteln kann. In diesem Fall würden Plexine nicht nur als Rezeptoren, sondern auch als Liganden, und Semaphorine nicht nur als Liganden, sondern auch als Rezeptoren fungieren. Wir haben diese neuartige Hypothese eines "reversen signalings" über Semaphorine experimentell überprüft. Tatsächlich konnten wir einen Signalweg charaktersieren, bei dem Plexin-B1 als Ligand und Semaphorin 4A (Sema4A) als Rezeptor die Migration und Invasion von Tumorzellen steuern. Durch eine Kombination massenspektrometrischer Analysen und siRNA-Screens konnten wir das Zellpolaritäts-Protein Scrib als Effektor von Sema4A indentifizieren. Die Bindung von Plexin-B1 an Sema4A fördert die Interaktion von Sema4A mit Scrib, entfernt Scrib dadurch aus einem Komplex mit dem Rac/Cdc42-auschtauschfaktor (GEF) βPIX, und vermindert die Aktivität der kleinen GTPasen Rac1 und Cdc42. Dieser Mechanismus operiert nicht nur in verschiedenen Tumorzellen, sondern auch in dendritischen Zellen, die Sema4A-abhängig in Richtung eines ansteigenden Gradierten von Plexin-B1 migrieren.
In laufenden Forschungsprojekten sollen die molekularen Kommunikationsnetzwerke in der Tumormikroumgebung („tumor microenvironment“) systematisch charakterisiert, und auf ihre funktionelle Relevanz für die Tumorprogression und -metastasierung überprüft werden. Wir konzentrieren uns hier neben dem Mammakarzinom insbesondere auf eine weitere gängige Tumorerkrankung, das Ovarialkarzinom. Das Ovarialkarzinom manifestiert sich zunächst auf eine Tumor-assoziierte der peritoneale Flüssigkeit aus, die neben Tumorzellen auch funktionell überaus bedeutsame Zelltypen – tumor-assoziierte Makrophagen und Tumor-assoziierte T-Zellen beinhaltet. Da das Ovarialkarzinom häufig sehr früh eine Transportfunktion von Signalmechanismen aus dem Tumor selbst in die Ascitesflüssigkeit aufweist, haben wir umfassende Analysen des Proteoms und Transkriptoms von aus dem Aszites von Ovarialkarzinom-Patientinnen isolierten tumor-assoziierten Tumorzellen, tumor-assoziierten Makrophagen und tumor-assoziierten T-Zellen durchgeführt. Wir konnten dabei verschiedene interzelluläre Signalwege identifizieren, die mit der Prognose der Patientinnen korrelieren. Insbesondere verschiedene interzelluläre Signalwege des Semaphorin-Plexin-Systems, aber auch anderer, bisher in diesem Zusammenhang unbekannter Signaltransduktionswege, konnten wir als funktionell relevante Kommunikationsachsen identifizieren. Unsere Ergebnisse weisen darauf hin, dass das Semaphorin-Plexin-System, aber auch andere, bishernicht in diesem Zusammenhang beschriebene Liganden-Rezeptor-pharmakoligische Zielstrukturen bei der Behandlung des Ovarialkarzinoms darstellen könnten.
Ausgewählte Publikationen:
- Jiang C, Javed A, Kaiser L, Nava MM, Zhao D, Brandt DT, Fernández-Baldovinos J, Zhou L, Höß C, Sawmynaden K, Oleksy A, Matthews D, Weinstein LS, Gröne HJ, Niessen CM, Offermanns S, Wickström SA, Worzfeld T. (2020).
Mechanochemical control of epidermal stem cell divisions by B-plexins.
bioRxiv. doi: https://doi.org/10.1101/2020.04.30.070359. - Worzfeld, T., Finkernagel, F., Reinartz, S., Konzer, A., Adhikary, T., Nist, A., Stiewe, T., Wagner, U., Looso, M., Graumann, J., Müller, R. (2018).
Proteotranscriptomics Reveal Signaling Networks in the Ovarian Cancer Microenvironment.
Molecular and Cellular Proteomics 17, 270–289 - Sun, T., Yang, L., Kaur, H., Pestel, J., Looso, M., Nolte, H., Krasel, C., Heil, D., Krishnan, R.K., Santoni, M.J., Borg, J.P., Bünemann, M., Offermanns, S., Swiercz, J.M., Worzfeld, T. (2017).
A reverse signaling pathway downstream of Sema4A controls cell migration via Scrib.
Journal of Cell Biology 216, 199–215 - Worzfeld, T., Swiercz, J.M., Looso, M., Straub, B.K., Sivaraj, K.K., Offermanns, S. (2012).
ErbB-2 signals through Plexin-B1 to promote breast cancer metastasis.
Journal of Clinical Investigation 122, 1296–1305