Hauptinhalt
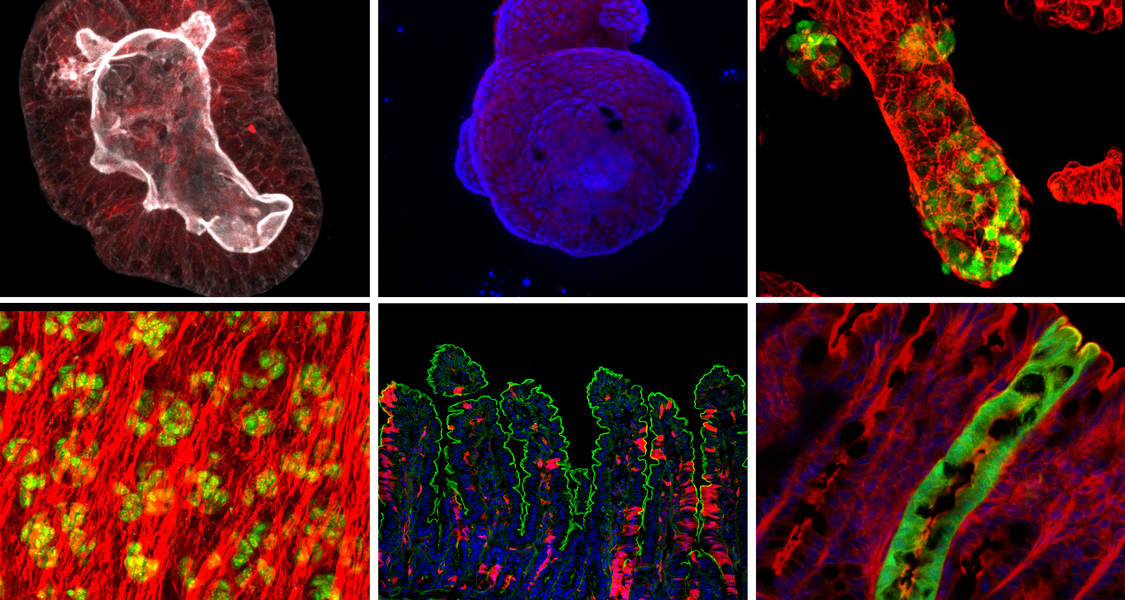
Die westliche Ernährungsweise, die sogenannte „Western-Style“ Diät ist einer der wichtigsten veränderbaren Risikofaktoren für Darmkrebs. In unserem Labor wollen wir herausfinden, wie genau Western-Style Diät das Darmkrebsrisiko erhöht und wie eine westliche Ernährung die Entwicklung von Darmtumoren und deren Therapierbarkeit beeinflusst. Auf diese Weise möchten wir neue Strategien zur Darmkrebsprävention und zur Verbesserung der Behandlung von Darmkrebs-Patienten entwickeln.