Hauptinhalt
Folgende Projekte werden in GLUE bearbeitet
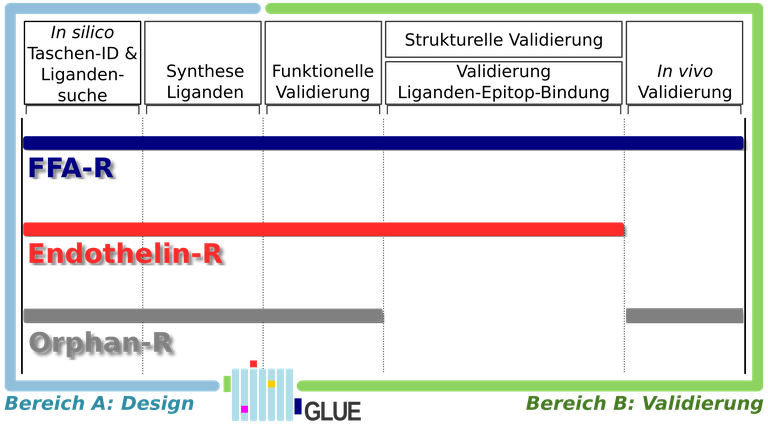
Projektbereich A | Design
A1: Strukturbasierte in silico Identifizierung von „druggable“ Epitopen und potenzieller Liganden an FFA, Endothelin- und GPRC5B (orphan) Rezeptoren (AG Kolb)
Hintergrund: Teilprojekt A1 besteht aus zwei Unterbereichen: der Identifizierung und Bewertung alternativer Epitope und der Identifizierung und Optimierung potenzieller Liganden.
Identifizierung alternativer Epitope. Der erste Schritt von GLUE ist die Bestimmung und Bewertung alternativer Kavitäten aller untersuchten Rezeptoren. Dies werden wir über Docking kleiner molekularer Sonden (z. B. Benzol, Dimethylether, Methan, Dimethylamin etc.) erreichen. Die dafür verwendete Software SEED generiert tausende Bindungsmodi für jede Substanz und erlaubt eine fundierte Bewertung jeder Tasche. Werden energetisch günstige Bindungsmodi gefunden? Binden alle Typen von Sonden (apolare, polare, geladene, etc.) gleich gut oder ergeben sich hier bereits Unterschiede? Welches Volumen weist die jeweilige Tasche auf? Diese „Landkarten“ werden wir schon frühzeitig mit den Forscherinnen und Forschern aus dem Projekt A2 teilen, mit dem Ziel, die Bewertung zu automatisieren und standardisieren. Die Etablierung wird anhand der vorhandenen Kristallstrukturen des FFAR1 und des ETB-R erfolgen. Zeitgleich werden wir die fehlenden Konformationen der drei Rezeptoren durch Homologiemodellierung erstellen.
Erweiterte Untersuchung alternativer Epitope. Kristallographisch klar aufgelöste, in mehreren Strukturen auftretende und fallweise bereits zuvor von Liganden in ähnlichen Rezeptoren adressierte Bindetaschen stellen klare erste Zielstrukturen dar. Ein prominentes Beispiel für eine solche Kavität ist die G-Protein-Bindetasche. Weniger wohldefinierte Taschen werden wir vor der weiteren Bearbeitung vertieft untersuchen. Neben erweiterten Sondenbibliotheken werden wir auch bioinformatische Methoden (z. B. Sequenzvergleiche) zum Einsatz bringen. Molekulardynamik-(MD)-Simulationen werden uns Aufschluss über die zeitaufgelöste strukturelle Stabilität der Taschen geben.
Screening mit kommerziell verfügbaren und noch nicht synthetisierten Molekülen. Unmittelbar nach der Definition der ersten bestbewerteten alternativen Epitope werden wir diese mit Docking und kommerziell erhältlichen Liganden passender Größe screenen. Ziel ist es, möglichst rasch erste Vorschläge für eine biophysikalische Evaluation und die medizinalchemische Entwicklung zur Verfügung zu stellen. In weiterer Folge werden wir den Fokus auf das Docking neuartiger, noch nicht synthetisierter Moleküle legen. Diese werden hauptsächlich aus drei Quellen stammen: (i) Designkonzepten der medizinalchemischen Kooperationspartnerinnen und -partner; (ii) unserer eigenen Datenbank synthetisch einfach zugänglicher Moleküle SCUBIDOO (iii) dem de novo Teil der Datenbank ZINC. Die durch Docking bestbewerteten potenziellen Liganden werden in weiterer Folge in A2 oder bei den jeweiligen Herstellern extern synthetisiert.
Optimierung bereits identifizierter Liganden. Sobald die ersten Liganden experimentell verifiziert worden sind, werden wir gemeinsam mit A2 an der strukturbasierten Optimierung der Liganden arbeiten. Dabei wird unsere Eigenentwicklung PINGUI zum Einsatz kommen, um nicht unmittelbar offensichtliche Synthesevorschläge auszuarbeiten. Wir werden danach trachten, sowohl die Affinität als auch die intrinsische Aktivität zu optimieren. Dies wird in einem mehrfach zu durchlaufenden Zyklus aus Design, Synthese und experimenteller Testung stattfinden.A2: Chemische Synthese und Optimierung niedermolekularer Liganden für identifizierte Epitope der FFARs, der blutdruckerhöhenden GPRC5B-Rezeptoren (alternativ GPR153) sowie der Endothelin-Rezeptoren (AGs Diederich, Schlitzer, Steinmetzer)
Hintergrund und Arbeitsprogramm: Ziel dieses Teilprojektes ist die Entwicklung, Synthese und Optimierung niedermolekularer Liganden für neue Bindetaschen der ausgewählten Rezeptoren.
Auswahl der zu adressierenden Bindetaschen. Pro Rezeptor werden initial zwei oder maximal drei der vom Teilprojekt A1 vorgeschlagenen Bindetaschen mit potentiellen Liganden adressiert. Durch ein erstes Screening kommerziell erhältlicher oder einfach herstellbarer Startstrukturen soll möglichst rasch die erfolgversprechendste allosterische Bindetasche an jedem Rezeptor identifiziert werden, auf die die weiteren Arbeiten fokussiert werden. Die vorgschlagenen Bindetaschen werden mit geeigneten Programmen aber auch manuell analysiert, um ihre Eignung für eine Wirkstoffentwicklung zu beurteilen und die identifizierten Startstrukturen zu verbessern.
Auswahl der Testverbindungen. Mittels Docking von Verbindungen verschiedener Wirkstoffdatenbanken werden erste potentielle Liganden für die entsprechenden Bindetaschen identifiziert. Basierend auf der Rangfolge der berechneten Bindungsstärke und Passgenauigkeit der Liganden in der Bindetasche werden die verfügbaren Verbindungen erworben und geprüft. Bei der Auswahl potentielle Liganden werden weitere Kriterien berücksichtigt, wie die Art ihrer intermolekularen Wechselwirkungen im Komplex mit dem Rezeptor, die strukturelle Variabilität ihrer Grundstruktur und auch deren synthetische Zugänglichkeit. Weiterhin sollen fragmentbasierte Ansätze mit schrittweiser Erweiterung des Ausgangsfragments genutzt, sowie individuelle Vorschläge nach visueller Inspektion der Bindetaschen durch die beteiligten Chemiker berücksichtigt werden. In Vorbereitung der Synthesearbeiten werden alle neu zu synthetisierenden Verbindungen unterstützend mittels Docking auf ihre Eignung geprüft.
Synthese erster Serien von Testverbindungen. Aus den durch die zuvor beschriebenen Verfahren identifizierten Molekülklassen werden die vielversprechendsten Strukturtypen ausgewählt und von jeder Klasse etwa 10 Beispielmoleküle synthetisiert. Dabei soll initial eine möglichst breite strukturelle Vielfalt abgedeckt werden, geringfügige Variationen werden auf später verschoben. Diese ersten Molekülserien werden von den Kooperationspartnern hinsichtlich ihrer Rezeptorbindung und biologischen Wirksamkeit geprüft. Sollte eines der dargestellten Moleküle die erwartete biologische Wirkung zeigen, wird dieser erste „Hit“ anschließend weiter optimiert.
Weiterentwicklung des Hits. Ausgehend von dem erhaltenen ersten Hit erfolgt eine klassische medizinalchemische Wirkstoffentwicklung, bei der durch aufeinanderfolgende Zyklen von durch Docking unterstütztem Design, Synthese und Testung die Verbindungen schrittweise optimiert werden. Durch mehrfache Wiederholung dieses iterativen Prozesses lassen sich immer genauere Struktur-Wirkungs-Beziehungen ableiten. Neben einer Verstärkung der biologischen Wirksamkeit werden in dieser Phase auch die pharmakokinetischen Parameter der besten Verbindungen geprüft und optimiert.
A3: Nachbarschaftsgestützes Screening von Typ A/B-hybriden GPCRs (AG Hausch)
Hintergrund. Peptidhormon-erkennende Typ B-GPCRs rekrutieren mittels einer speziellen extrazellulären Domäne den Erkennungsteil des Peptidhormons mit hoher Affinität und bringen damit den Aktivierungsteil des Peptids in die Nähe der Transmembrandomäne der GPCRs, die dadurch aktiviert werden. Basierend auf diesem Zwei-Stufen-Mechanismus entwickelten wir die Methode des biomimetischen Screenings zur Identifizierung neuer GPCR-Liganden.
Methodischer Ansatz. Zunächst werden Fusionskonstrukte für FFA2 und ETB1 mit der extrazellulären Domäne des CRF1-Rezeptors generiert. Die korrekte Lokalisation und Funktionalität dieser Konstrukte wird durch Fluoreszenz-Mikroskopie (mit B3) und zelluläre Assays (mit B1) nachgewiesen. Anschließend werden durch Verkürzung der bekannten Agonisten und Antagonisten minimale Liganden identifiziert, die gekoppelt an das Rekrutierungspeptid eine Stimulation oder Inhibierung der Rezeptoren bewirken und im weiteren Verlauf als Positiv-Kontrollen dienen. Zur Untersuchung von Typ A/B-Hybrid-GPCRs werden zwei Bibliotheken hergestellt: a) Festphasen-Synthese einer Acetylen-terminierten Peptid-Bibliothek und Konjugation an das Rekrutierungspeptid; b) Reaktion eines Thiol-haltigen Rekrutierungspeptids mit einer Sammlung aus Thiol-reaktiven Fragmenten.
Abschließend werden diese Bibliotheken bzgl. Aktivierung, Inhibierung oder allosterischer Verstärkung der endogenen Agonisten für die ETB1- und FFA2-Fusionskonstrukte getestet. Durch den quasi-intramolekularen Ansatz können anderweitig undetektierbare Substanzen identifiziert werden. Die Bindung der gefundenen Substanzen an die gereinigten GPCRs wird durch biophysikalische Studien bestätigt (mit B4), deren Bindungsmodus modelliert (mit A1) und ihr Effekt auf die Signaltransduktion in zellulären Assays charakterisiert (mit B1 & B3). Vielversprechende Hits werden medizinalchemisch optimiert (mit A2) und gegebenefalls in Primärzellmodellen getestet (mit B6).
Projektbereich B | Validierung
B1: Identifizierung der Ligandenbindung und biologischen Wirkung auf FFARs und Endothelin-R in zellbasierten Assays (AG Bünemann)
Hintergrund und Arbeitsprogramm. Das TP B1 hat die Aufgabe, die Bindung der im Projekbereich A entwickelten Liganden an die entsprechenden GPCRs nachzuweisen und deren funktionelle Wirkung zu charakterisieren. Hierfür werden zellbasierte Assays angewandt, die das Labor in der Vergangenheit auf Basis der Einzelzell- FRET-Mikroskopie entwickelt hat. Um möglichst umfassend potenzielle Wirkungen der entwickelten Liganden zu testen, ist geplant Assays zur Detektion der aktiven Rezeptorkonformation, sowie der Interaktion von Rezeptoren mit heterotrimeren G-Proteinen, Rezeptorkinasen und β-Arrestin sowohl für Endothelin- als auch FFA-Rezeptoren anzuwenden. Darüber hinaus werden potenzielle Liganden in Assays zur Detektion der G-Protein-Aktivierung getestet.
Liganden für FFA2- und FFA3 Rezeptoren. Wir werden von fluoreszenzmarkierten FFA-Rs entwickeln sowie Rezeptorsensoren zur Detektion ihrer Liganden-induzierten Konformationsänderungen etablieren. Mittels FRET-basierten Assays zur Signaltransduktion, insbesondere den Interaktionsassay von GPCR und G-Protein unter nukleotidfreien Bedingungen werden wir die Teilbereich A vorgeschlagenen Liganden bezüglich ihrer Wirkung auf die jeweiligen Rezeptoren testen. Um einen höheren Probendurchsatz zu gewährleisten sollen BRET und z.T. auch FRET-Assays im Plattenreader angewendet und optimiert werden. Schwerpunkt ist die tiefgreifende Charakterisierung von GLUE- Liganden bezüglich deren funktionaler Wirkung auf die GPCRs. Mit TP B6 sollen zusätzlich Ca2+- und cAMP-Imaging Assays zur Untersuchung von FFA-Rezeptoren in Primärzellen aufgesetzt werden.
Analog zum Projekteil A werden ETB-Rezeptoren und GPRC5-Rezeptoren primär mittels FRET-Mikroskopie-basierter Assays untersucht. Zusätzlich soll in Zusammenarbeit mit B4 versucht werden FRET/BRET-basierte Interaktionsassays mit in vitro-translatierten Rezeptoren zu etablieren, sowie diese in intakten Zellen zu rekonstruieren und dann mit funktionellen Assays zu vermessen. Weiterhin soll die Rezeptordimerisierung von Endothelinrezeptoren sowie GPCR5b-Rezeptoren mittels FRAP Analysen in enger Zusammenarbeit mit B2, B3 und B7 analysiert werden.B2: Analyse von Rezeptorkomplexen und der Einfluss von Liganden mittels Massenspektrometrie (AG Morgner)
Hintergrund. Native Massenspektrometrie (MS) erlaubt die Untersuchung nicht-kovalent gebundener Proteinkomplexe aus wässriger Lösung. Wir haben dazu eine Ionenquelle entwickelt, die speziell für die Untersuchung von Membrankomplexen geeignet ist. Diese Methode (LILBID – Laser Induced Liquid Bead Ion Desorption) nutzt Mikrotröpfchen des Analyten, die mit einem Infra-Rot-Laser desorbiert werden, um die Ionen freizusetzen. In diesem Desorptionsprozess werden Detergenzien oder unspezifisch gebundene Lipide von den Proteinen gelöst, sodass nun die MS-Analyse der Membranproteine und ihrer Komplexe möglich ist. Dies erlaubt deren Untersuchung aus Detergenzien oder auch nativeren Umgebungen, wie Nanodiscs. Kürzlich ist es uns gelungen, auch Membranproteinkomplexe aus sogenannten SMALPS mit LILBID zu untersuchen 2. Dazu werden die Proteinkomplexe mit einem Teil ihrer nativen Lipid-Umgebung mit Hilfe von SMA (styrene maleic acid) Co-polymeren direkt aus der Zelle ausgelöst. Die so gewonnen SMALPs (SMA lipid particles) können wir direkt zur Analyse der Proteinstöchiometrie nutzen.
Arbeitsprogramm. Wir beabsichtigen, mit der Untersuchung von FFA1-Rezeptoren zu beginnen. Diese sollen in Zusammenarbeit mit der Gruppe Dötsch/Bernhard durchgeführt werden. Geplante Untersuchungen in Zusammenarbeit mit anderen Gruppen aus dem Konsortium beinhalten die Lipid-abhängige Dimerisierung von z.B. FFA1-Rezeptoren, welche zellfrei in Nanodiscs exprimiert werden (Frank Bernhard). Die Lipidzusammensetzung dieser Discs kann variiert werden, um den Einfluss auf den Oligomerisierungszustand sowie die spezifisch gebundenen Lipide zu analysieren.
Solche Proben sollen dann mit in vivo-Proben verglichen werden. Dazu wollen wir SMALPs nutzen, die die FFA1-Rezeptoren mit ihren umgebenden Lipiden enthalten. Die Bestimmung der Stöchiometrie sowie potenzieller Co-Faktoren ist mit jetziger Technologie möglich. Unabhängig von GLUE arbeiten wir an LILBID mit verbesserter Massenauflösung. Dadurch werden wir in naher Zukunft auch die Möglichkeit haben gebundene Lipide zu untersuchen.
Eine weitere Fragestellung, die wir adressieren wollen, ist die Bindung von Liganden, die qualitativ untersucht werden kann. Im Fokus stehen hier allosterische Liganden, und deren Einfluss auf die GPCR Oligomerisierung. Mutationen (in Kollaboration mit B4) an potenziellen Bindestellen von Liganden erlauben die Analyse der exakten Bindestellen und Unterschiede im Bindungsverhalten, sowie die Unterscheidung von allosterischer Unterbindung von Ligandenbindung im Gegensatz zu Verdrängung.
Sobald weitere GPCR-Proben aus dem Konsortium zur Verfügung stehen, sollen diese auf ähnliche Fragestellungen hin untersucht werden. Geplant ist hier die Zusammenarbeit mit B1, B3 und B7 in Bezug auf GPRC5b und GPR153.In einem parallel laufenden Projekt soll die quantitative Bestimmung von Bindungskonstanten mittels Massenspektrometrie etabliert werden. Hierzu muss zunächst der Energietransfer des LILBID-Desorptionslasers genau bestimmt werden. In Abhängigkeit der Laserstärke soll dann die laserinduzierte Proteinkomplex-Dissoziation beobachtet werden, um daraus Rückschlüsse auf die Bindungsstärke ziehen zu können. Wir beabsichtigen, diese Methode für die Analyse von Membranproteinen anzupassen, um damit Bindungskonstanten für die Bindung der GPCR Dimere sowie deren Liganden bestimmen zu können.
B3 Einzelmolekül-Mikroskopie basierte Untersuchungen der Aktivität von GPCRs nach Modulation durch allosterische Liganden (AG Meckel)
Hintergrund. Mit kaum mehr als 3.000 Kopien pro Zelle ist die endogene Expression von GPCRs in Säugerzellen sehr gering. Solch niedrige endogene Expressionsniveaus stellen eine Herausforderung für viele biochemische Analysemethoden dar, die im Rahmen von Wirkstoff-Screenings Anwendung finden. Eine Lösung liegt daher oft in der Herstellung von Zelllinien, die eine wesentlich höhere Expression an GPCRs haben. Während solche Zelllinien im Rahmen von Strukturstudien, beim Screening neuer Liganden oder bei der Generierung funktioneller Antikörper gegen GPCRs ihre Berechtigung haben, sind sie für zellphysiologische Untersuchungen zur funktionellen Validierung neuer Wirkstoffkandidaten weniger geeignet. Gerade bei GPCRs, deren Funktionsweise auf der Formierung des ternären Komplexes beruht, sind Expressionsniveaus alles andere als unerheblich. Mit der Einzelmolekül-mikroskopie steht jedoch eine Methode zur Verfügung, die bestens geeignet ist, GPCRs bei physiologisch relevanten Expressionsniveaus zu charakterisieren.
Ziele. (1) Erfassen und Vergleich des Anteils aktiver GPCRs (FFA2, FFA3, ETB, GPRC5b) sowie der Häufigkeit und Lebensdauer der ternären Komplexe in Gegenwart (i) bekannter orthosterischer Agonisten und Antagonisten sowie (ii) in zusätzlicher Gegenwart neuer allosterischer Liganden (mit A2). (2) Untersuchung der Dimerisierung (B2 und B7) und ggf. Clusterung von GPCRs (insbesondere GPRC5b) sowohl an 2D und 3D kultivierten Zellen als auch an Primärgewebe aus Mäusen (B6 und B7).
Arbeitsprogramm. Zur transienten Transfektion von HEK293 Zellen mit CLIP- und SNAP-tag markierten GPCRs und G-Proteinen werden mono-, bi- und tricistronische Plasmide erstellt (mono: CLIP-GPCR, bi: Gα-SNAP + Gβγ, tri: alle drei). Parallel dazu werden stabile Zelllinien (CRISPR/Cas9) mit denselben Konstrukten, jedoch Tetracyklin-induzierbaren Promotoren (TRE) hergestellt. Die Funktionalität dieser Konstrukte und Zelllinien wird durch FRET-basierte Assays überprüft (B1). Eine dritte Möglichkeit, zur Untersuchung geringer GPCRs Level ist der Einbau von Nanodisks in Zellmembranen. Diese Möglichkeit wird mittels Einzelmolekül-Mikroskopie evaluiert und quantifiziert (mit B4). Die Färbung der Zellen mit zell-impermeablen CLIP-Substraten (CLIP-Surface® 488, 547, 647) und zell-permeablen SNAP-Substraten (SNAP-Cell® 647-SiR) sowie die Einzelmolekül-Mikroskopischen Untersuchungen werden 3-6 h nach der Transfektion durchgeführt, um die Expressionslevel niedrig zu halten. Um den optimalen Zeitpunkt für Messungen nach der Transfektion bzw. den Grad der Aktivierung des TRE Systems zu bestimmen, wird die Abundanz, Multimerisierung und Clusterung der GPCRs und G-Proteine an fixiertem und immunmarkiertem Primärgewebe aus Mäusen (B6 und B7) mittels Einzelmolekül-Lokalisations-Mikroskopie quantifiziert. Schließlich wird die Mobilität und damit die Aktivität der Fluoreszenz-markierten GPCRs und G-Proteine durch Einzelmolekül-Tracking in Gegenwart der verschiedenen Liganden analysiert. Zudem wird die Verlangsamung einzelner Proteine und durch simultanes Tracking zweier Proteine (CLIP-GPCR, Gα-SNAP) die Interaktions-Häufigkeit und -Dauer festgehalten.
B4: Biochemische und strukturelle Untersuchung von Wechselwirkungen von Liganden mit FFAR und Endothelin-R (AG Bernhard/Dötsch)
Hintergrund: Die Kombination zellfreier Produktion mit der Nanodisctechnologie ist ein effizienter Ansatz zur Synthese von GPCRs in vorgefertigte definierte Membranen. Die funktionelle Faltung der GPCRs wird durch Ligandenbindung quantifiziert und systematisch durch modifizierte Reaktionsbedingungen auch in Durchsatzverfahren optimiert.
Der etablierte Prozess der zellfreien ETB Synthese soll als Plattform zur Identifizierung und Bindungsanalyse neuer Liganden eingesetzt werden. Aufgrund der Zugänglichkeit des GPCRs können intra- bzw. extrazelluläre Rezeptorbereiche simultan oder exklusiv adressiert und auch allosterische Effekte analysiert werden.Arbeitsprogramm: Basierend auf der ETB/ET-1 Struktur modellierte (A1) und synthetisierte (A2) Liganden sollen zunächst auf Bindung und Kompetition zu ET-1 und Derivaten davon untersucht werden. Zusätzliche strukturelle Informationen von Interaktionen sollen mittels Festkörper NMR (B5) erhalten werden.
Die in vitro Untersuchungen von GPCR/Liganden Interaktionen sollen mit in vivo Funktionen des GPCRs gekoppelt werden. Ermöglicht wird dies durch eine neue Methode zur Fusion von Nanodisc Membranen mit Membranen lebender Zellen. Daten aus in vitro Studien könnten dadurch im komplexen zellulären Kontext verifiziert und mit in vivo Analysen erweitert werden. Die Mechanismen dieses Nanotransfers sind noch weitgehend unklar und grundlegende Parameter müssen zunächst identifiziert und Lokalisation und Stabilität transferierter GPCRs mit Hilfe von Einzelzell-Analyse (B3) optimiert werden. Bereits vorhandene Zell-Linien mit G-Protein Reporterfusionen sollen anschließend für Nanotransfer Experimente mit zellfrei hergestellten GPCR/ Nanopartikeln (Nanodiscs, Salipros, DIBMaLPs) eingesetzt werden (B1).
Insbesondere zunächst nur schwach bindende Liganden sollen durch die Methode des nachbarschaftsgestützten Screenings mit Hilfe chimärer Konstrukte aus ETB und CRF1 identifiziert werden (A3). Größere Molekülbibliotheken können hierzu mit unserem Durchsatzprozess analysiert und identifizierte Liganden systematisch auf molekularer Ebene optimiert werden (A1, A2). Alternativ zu Radioassays sollen Bindungsassays mit fluoreszenzmarkierten Derivaten von ET-1 (A2) etabliert und eingesetzt werden. Speziell zur Identifizierung intrazellulärer Liganden soll die Verdrängung fluoreszenzmarkierter Nanobodies, die an intrazelluläre Epitope von GPCRs binden, etabliert werden. Alternativ soll die Ligandenbindung und deren Effekt auf die GPCR Oligomerisierung mittels nativer Massenspektrometrie (B2) untersucht werden.
Unsere Syntheseplattform kann auf andere GPCRs, z.B. FFAR, transferiert werden (A3, B6, B7). Faltungsrelevante Parameter können sukzessive optimiert und die erfolgreiche co-translationale Insertion in unterschiedliche Nanopartikel auch unabhängig von verfügbaren Liganden zunächst mit Hilfe von GPCR-GFP Fusionen und Massenspektroskopie (B2) untersucht werden. Die NMR Analyse (B5) erfordert zudem weitere stabilisierende Modifikationen von ETB.B5: NMR-Spektroskopische Untersuchungen zu molekularen Mechanismen der Ligandenbindung an GPCRs (AG Glaubitz)
Hintergrund: In diesem Projekt werden wir NMR Spektroskopie verwenden, um neue Ligandenbindungsmoden an GPCRs zu analysieren. Wir setzen hierbei insbesondere auf Festkörper-NMR Spektroskopie. Die Detektionsempfindlichkeit wird durch den Einsatz der dynamischen Kernpolarisation, einem neuen NMR/EPR-Hybridverfahren, erhöht. Der Schwerpunkt dieses Teilprojektes liegt zunächst auf Festkörper-NMR Studien am Endothelin-B Rezeptor, dessen Präparation mittels zellfreier Expressionstechniken in B4 in den letzten Jahren erfolgreich etabliert wurde.
Arbeitsprogramm: Zunächst sollen geeignete NMR Experimente und Markierungsschema am ETB allein und im Komplex mit seinem Agonisten Endothelin-1 (ET1) erarbeitet werden. Am Rezeptor soll zunächst eine Reste-spezifische Markierung erfolgen, so dass ein 2D-„Fingerprintspektrum“ erhalten werden kann. Eine Resonanzzuordnung erfolgt über kombinatorische, paarweise Markierung benachbarter Reste. Aus der Analyse der Spektren unter Ligandentitration kann auf strukturelle und dynamische Veränderungen in ETB geschlossen werden. Da die orthosterische Bindestelle bekannt ist, können Markierungen auch so gewählt werden, dass auch Reste in der Bindetasche abdeckt werden. Im Komplex mit 13C-15N-ET1 könnten somit mittels Festkörper-NMR direkte Interaktionen zwischen Agonist und GPCR visualisiert werden. ETB wird durch eine Reihe verschiedener Agonisten aktiviert. Aus den „Fingerprintspektrum“ der entsprechenden Komplexe ließe sich ableiten, ob der Rezeptor unterschiedliche Konformationen annimmt und/oder ob sich das Gleichgewicht zwischen verschiedenen Konformeren verschiebt. Für diese Studien wird ETB in Liposomen rekonstituiert. Die Information aus den NMR Spektren kann auch verwendet werden, um den Einfluss verschiedener Membranumgebungen (Liposomen, Nanodiscs, SMALPS siehe B4), auf die Rezeptorkonformation zu untersuchen. Die so etablierten experimentellen Ansätze werden nun auf neue Bindungsepitope angewendet. Basierend auf den ETB Kristallstrukturen soll in A1 eine Suche nach alternativen Epitopen durchgeführt sowie neuartige Liganden (A2) vorgeschlagen werden. Die Anzahl möglicher „Hits“ soll zunächst durch biochemische Assays eingeengt werden (B1, B4). Basierend auf den besten Vorhersagen und verfügbaren Liganden sollen nun NMR-Studien durchgeführt werden um zu verifizieren, ob eine Ligandenbindung zu Konformationen in ETB führt, die denen bei Besetzung der orthosterischen Bindungsstelle entspricht.
Ergänzend zu den geplanten Arbeiten am ETB Rezeptor sollen aufbauend auf unseren Vorarbeiten unsere Modelle für die humanen Bradykinin-1 und 2 Rezeptoren (B1R, B2R) durch A1 hinsichtlich neuer Bindungsepitope analysiert werden. Bei positiver Vorhersage entsprechender Bindungsstellen und bei Verfügbarkeit geeigneter Liganden (A2) können entsprechende Bindungsstudien auch an diesen Rezeptoren mit in das Programm aufgenommen werden. Hierfür würden die Rezeptoren in Sf9 hergestellt werden. Ebenso können unsere NMR Studien auf FFAR ausgedehnt werden, wenn dieser Rezeptor in der Laufzeit des Projektes in stabiler und funktionaler Form hergestellt werden kann.
Methodenentwicklung: Neben den beschriebenen Anwendungen sollen auch neue methodische Entwicklungen vorangetrieben und deren Anwendbarkeit auf GPCR-Ligandenkomplexe validiert werden. (a) DNP-verstärkte Festkörper-NMR mit lokalisierter Signalverstärkung: Durch spezifische Methylgruppenmarkierung am Rezeptor oder am Liganden soll eine DNP-Signalverstärkung nur lokal erzeugt werden. Damit lassen sich vereinfachte Spektren erhalten, in denen bereits Informationen zur räumlichen Nähe von Ligand und Resten in der Bindungstasche kodiert sind. (b) Festkörper-NMR mit direkter Protonendetektion: Eine Voraussetzung für DNP-NMR sind Experimente bei tiefen Temperaturen (100 K). Dies bringt viele Vorteile mit sich, schränkt aber auch die Auflösung der NMR Spektren etwas ein. Herkömmliche Festkörper-NMR hingegen kann bei sehr großen Magnetfeldern und beliebigen Temperaturen durchgeführt werden, so dass alle Resonanzen von 7-TM Rezeptoren aufgelöst werden können wie bspw. von uns demonstriert. Für Anwendungen auf GPCRs mit reduzierten Probenmengen wäre allerdings eine höhere Empfindlichkeit nötig. Ein neuer technischer Ansatz für dieses Problem basiert auf direkter Protonendetektion (statt 13C oder 15N) mit Hilfe von sehr schneller Probenrotation (110 kHz). Im Rahmen dieses Projektes werden wir derartige Experimente an GPCRs etablieren und Vor- und Nachteile gegenüber DNP-verstärkter MAS NMR evaluieren.B6: In vivo-Funktionen und allosterische Regulation von FFA-Rezeptoren (AG Offermanns)
Hintergrund: Fettsäurerezeptoren (FFAs) sind eine Untergruppe von G-Protein-gekoppelten Rezeptoren, die in die Steuerung insbesondere metabolischer und immunologischer Prozesse involviert sind. Zu den FFA-Rezeptoren gehören Rezeptoren für kurzkettige Fettsäuren wie FFA2 und FFA3. Sowohl für FFA2 als auch für FFA3 ist eine kritische Rolle bei der Regulation der Insulinfreisetzung gezeigt worden, während FFA2 auch an der Steuerung von entzündlichen Prozessen beteiligt ist. Diese spezifischen Funktionen von FFA-Rezeptoren machen sie zu interessanten Zielstrukturen für Pharmaka für die Beeinflussung immunologischer, entzündlicher und metabolischer Prozesse. In den bisherigen Untersuchungen haben wir insbesondere die physiologische und pathophysiologische Funktion von FFA2 und FFA3 bei der Steuerung der Insulinsekretion untersucht. Im Rahmen dieser Arbeiten haben wir konditionale Allele der die Rezeptoren FFA2 und FFA3 kodierenden Gene in der Maus generiert und in vitro- sowie ex vivo-Systeme zur Untersuchung dieser Rezeptorfamilie etabliert.
Arbeitsprogramm: In dem hier beantragten Projekt sollen, aufbauend auf Voruntersuchungen sowie dem erheblichen pharmakologischen Potenzial dieser Rezeptorfamilie, in Zusammenarbeit mit den Teilprojekten A1-2, B1-B4 allosterische Modulatoren dieser Rezeptoren entwickelt und pharmakologisch charakterisiert werden. Dabei liegt der Schwerpunkt auf der in vitro- und in vivo-Testung antagonistisch bzw. negativ-allosterisch wirksamer Liganden für FFA2 und FFA3. Um die physiologischen und möglicherweise pathophysiologischen Funktionen von FFA2 und FFA3 genauer zu untersuchen, sollen unter Nutzung der bereits generierten konditionalen Allele beider Gene konditionale Knockouts von FFA2 und FFA3 in α-Zellen, enteroendokrinen Zellen und von FFA2 in Adipozyten und myeloischen Zellen unter Verwendung entsprechender, bereits vorhandener Cre-Linien generiert und analysiert werden. Die Untersuchung der Tiere soll sich zunächst auf metabolische Funktionen wie die Regulation der Insulinfreisetzung unter physiologischen und pathophysiologischen Bedingungen und die Entwicklung und Progression einer Adipositas konzentrieren. Schließlich werden wir neuartige allosterisch wirkende Liganden an FFA2 und FFA3, die in A1-2 generiert wurden, in in vitro-Systemen mit heterologer Expression von FFA2 und FFA3 auf ihre pharmakologischen Eigenschaften hin vergleichend mit anderen bekannten Liganden untersuchen. Sollten es die Eigenschaften neuer Liganden zulassen, so sollen diese auch in Tierexperimenten analysiert werden, wobei auch hier die Steuerung der Insulinsekretion (FFA2 und FFA3) oder inflammatorische Modelle (FFA2) im Zentrum stehen werden. Parallel zu den ex vivo und in vivo durchgeführten Experimenten werden wir in Zusammenarbeit mit den Teilprojekten B1 und B3 den molekularen Mechanismus der Rezeptorbindung vielversprechender neuer FFA-Rezeptor-Liganden durch Untersuchungen an Rezeptoren mit Punktmutationen zunächst in vitro analysieren. Gegebenenfalls werden mittels CRISPR/Cas9-vermittelter Geneditierung in fertilisierten Oozyten entsprechende Punktmutationen in das den entsprechenden FFA-Rezeptor kodierende Gen für in vivo-Analysen eingeführt werden.B7: Analyse der biologischen Funktion und pharmakologischen Modulierbarkeit von GPRC5B (bzw. GPR153) in vitro und in vivo (AG Wettschureck)
Hintergrund: GPRC5B wurde von uns in einer vaskulären Einzelzellexpressionsanalyse als einer derjenigen Rezeptoren identifiziert, die möglicherweise eine Rolle bei der krankhaften Entdifferenzierung von Glattmuskelzellen sowie der Endothel-Aktivierung im Rahmen der Atherosklerose spielen. GPRC5B gehört zur Klasse C der GPCRs; momentan sind weder endogener Ligand noch intrazelluläre Signaltransduktion bekannt. Um die Rolle dieses Rezeptors zu untersuchen, etablierten wir knockdown-Zellkulturmodelle und stellten gewebespezifische Knockout-Mäuse her. Unsere bisherigen Untersuchungen in kultivierten Zellen und isolierten Gefäßen deuten darauf hin, dass GPRC5B angiogenetische Prozesse in Endothelien sowie Glattmuskelkontraktilität reguliert; darüber hinaus gibt es in der Literatur Hinweise auf eine Funktion bei der Regulation von Insulinsekretion und metabolisch bedingter Entzündung. Ein weiterer im Rahmen unserer vaskulären Einzelzellexpressionsanalyse identifizierter Rezeptor ist GPR153, ein Orphan-GPCR der Klasse A. Vorläufige in vitro-Untersuchungen zeigen, dass GPR153 in Endothelien eine Rolle bei der Regulation von Inflammation und Angiogenese spielt, ansonsten ist nichts über die Funktion dieses Rezeptors bekannt. Globale GPR153-Knockout-Mäuse sind nicht lebensfähig, zelltypspezifische Knockouts werden momentan per CRISPR/Cas-Genomeditierung in unserer Gruppe hergestellt.
Primäres Ziel des Projektes ist es, die Funktionen des Orphan-Rezeptors GPRC5B zu charakterisieren und Liganden für eine pharmakologische Modulation des Rezeptors zu identifizieren. Sollten sich bei der Rezeptormodellierung und Ligandenentwicklung unerwartete Schwierigkeiten ergeben, soll GPR153 als Alternativprojekt in den Fokus rücken.Arbeitsprogramm: Charakterisierung der Funktion von GPRC5B und GPR153 in Primärzellen und in konditionalen Knockout-Mäusen: In der ersten Hälfte der Förderperiode werden wir die Rolle der beiden Orphan-Rezeptoren in Zellen des kardiovaskulären und endokrinen System ex vivo und in vivo definieren und ihre intrazelluläre Signaltransduktion aufklären. Schwerpunkte sind hierbei die Rolle von GPRC5b bei der Insulinsekretion und der Regulation der Gefäßkontraktilität; im Falle von GPR153 liegt der Fokus zunächst auf der Endothelfunktion. Diese Untersuchungen werden die methodologische Grundlage für die Testung der im Rahmen des Konsortiums identifizierten Modulatoren schaffen.
Testung von GPCR-Modulatoren in Primärzellen: Die im Rahmen des Konsortiums durch Modellierung von potenziellen Bindetaschen identifizierten (A1), synthetisierten (A2) und auf Wirksamkeit in Zelllinien getesteten (B1, B2, B3) Liganden werden hier auf ihre Wirksamkeit in wildtypischen und Rezeptor-defizienten humanen und murinen Primärzellen untersucht.
Als Testsystem dienen dabei die unter 1) identifizierten physiologischen Funktionen der Rezeptoren, beispielsweise GPRC5B-vermittelte Kapillarbildung in kultivierten Endothelzellen. Diese kann anhand der Neigung zur Röhrenbildung bestimmt werden und ist in GPRC5B-defizienten Endothelzellen reduziert. Es soll nun untersucht werden, ob die putativen Liganden die Röhrenbildung in wildtypischen, nicht aber GPRC5B-defizienten Endothelzellen positiv oder negativ beeinflussen. Je nach Verlauf der Untersuchungen in 1) sollen hier auch andere Testsysteme zum Einsatz kommen, beispielsweise Kontraktilität von Glattmuskelzellen oder Insulinsekretion in pankreatischen beta-Zellen.Testung von GPCR-Modulatoren in vivo: Bei vielversprechenden Ergebnissen in Primärzellen und erfolgreicher pharmakokinetischer und toxikologischer Charakterisierung werden wir die Effekte der Modulatoren in vivo im Mausmodell analysieren. Die Auswahl des in vivo-Modelles wird sich nach den bis dahin erhobenen Daten zur physiologischen Relevanz von GPRC5B richten; es stehen beispielsweise murine Testsysteme für Angiogenese, Blutdruckregulation (B6) oder Insulinsekretion/Diabetesentwicklung zur Verfügung. Um die Spezifität der Modulatoren für GPRC5B nachzuweisen, können diese Untersuchungen parallel in Rezeptor-Knockout-Linien erfolgen, bei denen die Substanzen ohne Effekt sein sollten.
Gemeinsam werden diese Versuche Auskunft darüber geben, ob die vom Konsortium identifizierten Modulatoren in der Lage sind, (patho-)physiologisch relevante Prozesse ex vivo und in vivo zu beeinflussen.