31.07.2020 „Science“-Artikel: Bruchstelle verlangsamt Blutzucker-Stoffwechsel
Internationales Team mit Marburger Beteiligung klärte die Struktur eines Hormonrezeptors auf
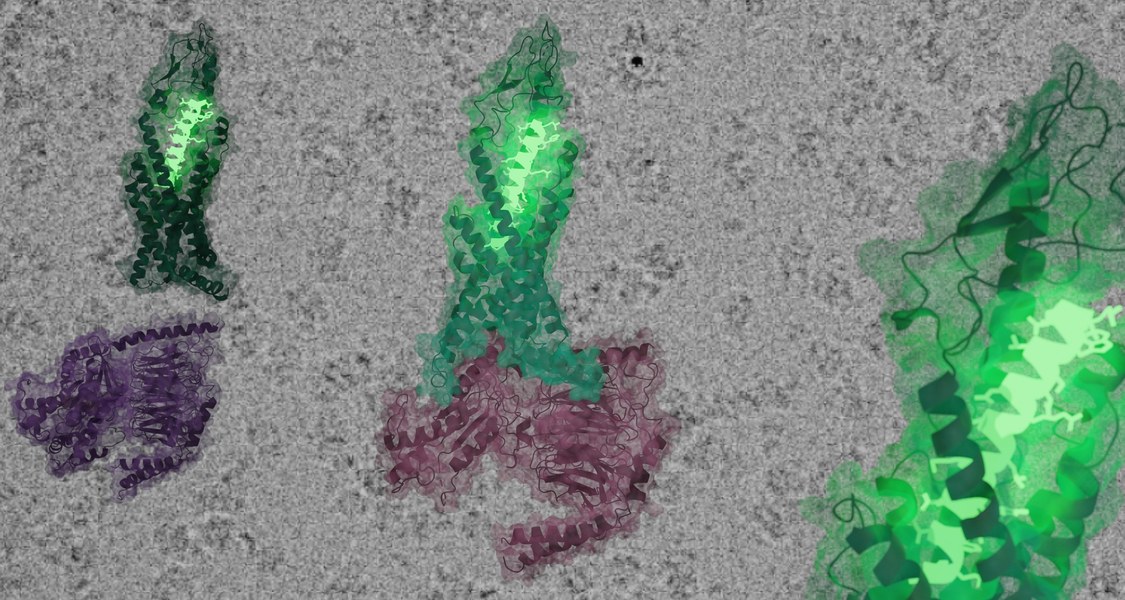
Nachzuckern? Immer mit der Ruhe! Die Steuerung des Blutzuckerspiegels geht an einer entscheidenden Schaltstelle langsamer vor sich als vergleichbare hormonelle Vorgänge. Das ergibt sich aus der Struktur und Funktion des Rezeptors, der auf die Ausschüttung des Hormons Glucagon reagiert – er übersetzt diese in eine zelluläre Antwort, die zu einem Anstieg des Blutzuckerspiegels führt, aber mit Verzögerung. Ein internationales Forschungsteam um den Marburger Biologen Dr. Daniel Hilger hat den Rezeptor genau unter die Lupe genommen; es berichtet im Wissenschaftsmagazin „Science“ über seine Ergebnisse.
Das Hormon Glucagon steuert den Blutzuckerspiegel, der krankhaftes Übergewicht und Diabetes beeinflusst. Schüttet die Bauchspeicheldrüse das Hormon aus, so führt dies über eine komplizierte Abfolge molekularer Wechselwirkungen dazu, dass Zucker freigesetzt wird. Zu Beginn steht dabei die Kopplung von Glucagon an seinen Rezeptor, der in der Zellmembran verankert ist. „Wegen seiner grundlegenden Rolle beim Glukose-Stoffwechsel bietet sich der Rezeptor als Ziel für die Behandlung von Patienten an, die an Diabetes oder krankhaftem Übergewicht leiden“, sagt Daniel Hilger, der maßgeblich an der Forschungsarbeit mitwirkte.
Sobald Glucagon auf der Zelloberfläche an den Rezeptor koppelt, stößt dieser im Zellinneren eine Kaskade von Reaktionen an, die schließlich eine erhöhte Zuckerabgabe ins Blut zur Folge hat. Der kettenförmige Rezeptor besitzt 7 Transmembrandomänen, die die Zellmembran durchlaufen um den Rezeptor in dieser zu verankern. Das kettenförmige Rezeptormolekül ist in eine Vielzahl von Schlaufen gelegt, die den Rezeptor in der Zellmembran verankern. Die Wissenschaftlerinnen und Wissenschaftler um Hilger klärten die Struktur des Rezeptors mittels Kryo-Elektronenmikroskopie auf, bei der die Moleküle stark gekühlt werden. „Wir haben ein künstliches Glucagonmolekül mit verbesserter Löslichkeit hergestellt, das wir in Komplex mit dem Rezeptor untersuchten“, erklärt Hilger, der diese Forschungsarbeiten noch in seiner Zeit an der Stanford Universität in den USA durchführte.
Eine der Molekülschlaufen Transmembrandomänen enthält eine ausgeprägte Bruchstelle; sie kommt bei verwandten Rezeptoren für andere Botenstoffe nicht vor – ein Unterschied, der nicht ohne Folgen bleibt: Dadurch verlangsamt sich offenbar die Aktivierung der Proteine, die im Zellinneren nachgeschaltet sind.

„Das Glucagon-Hormon hat eine starke Tendenz, an den Rezeptor zu koppeln und dort zu verbleiben“, erläutert der Biologe. Das könnte dazu führen, dass der Blutzuckerspiegel immer weiter steigt. „Wir vermuten, dass durch die erschwerte Aktivierung der nachgeschalteten Signalproteine eine bessere Kontrolle des Blutzuckerspiegel-Anstiegs ermöglicht wird“.
Die Gruppe analysierte auch noch weitere Proteine derselben Rezeptorfamilie. „Die Ergebnisse legen nahe, dass die beobachteten Unterschiede sich für die gesamte Klasse verwandter Rezeptoren verallgemeinern lassen“, berichtet Hilger. Wenn man Wirkstoffe finde, die die Bruchstelle stabilisieren, so könne dies ganz neue Möglichkeiten für Therapien eröffnen, vermutet der Gruppenleiter – zum Beispiel bei Diabetes und krankhaftem Übergewicht.
Der Biologe Dr. Daniel Hilger leitet eine Forschungsgruppe am Fachbereich Pharmazie der Philipps-Universität. Die Veröffentlichung entstand noch im Labor des Chemie-Nobelpreisträgers Professor Dr. Brian Kobilka an der Stanford Universität. Neben Hilger beteiligten sich weitere Wissenschaftlerinnen und Wissenschaftler der Stanford Universität sowie anderer Forschungsinstitutionen aus den USA, Dänemark und Japan an der Studie. Der Deutsche Akademische Austauschdienst und eine Reihe von Förderorganisationen unterstützten die Forschungsarbeit finanziell.
Originalveröffentlichung: Daniel Hilger, Kaavya Krishna Kumar, Hongli Hu & al.: Structural insights into differences in G protein activation by family A and family B GPCRs, Science 2020, DOI: 10.1126/science.aba3373