Hauptinhalt
Ionisierungstechniken
Zur Verfügung stehen derzeit folgende Ionisierungstechniken:
Inhalt ausklappen Inhalt einklappen Vergleich der Ionisierungstechniken
ESI "soft" ionization
"no" fragmentation
(exception: Skimmer-fragmentation or targeted fragmentation methods like CID, ETD)Multiply charged molecular ions
(rule of thumb: 1 charge/1000 mass units)Observation of non-covalent complexes possible
Direct coupling with HPLC
Also TLC-MS
APCI "soft" ionization
"no" fragmentation
(exception: Skimmer-fragmentation or targeted fragmentation methods like CID)Singly charged molecular ions(!)
Observation of non-covalent complexes possible
Direct coupling with HPLC
Also TLC-MS
MALDI "soft" ionization
"no" fragmentation
(exception: targeted TOF/TOF-fragmentation)Singly charged molecular ions "Offline" coupling with HPLC EI "hard" ionization
Servere fragmentation
radical fragment ions, partially molecular ions
Identification of known compounds by database search
Direct coupling with GC CI "soft" ionization
no or little fragmentation
Singly charged ions, mainly molecular ions Direct coupling with GC FD/LIFDI/FI "soft" ionization Singly charged molecular ions Direct coupling with GC (FI) Inhalt ausklappen Inhalt einklappen EI (Electron Impact)

Bei der EI-Ionisierung wird die Probe im Hochvakuum des Massenspektrometers in der Regel durch Erhitzen verdampft. Die in der Ionisierungskammer verdampften Analytmoleküle durchqueren einen Elektronenstrahl, wobei sie ein Elektron verlieren und in der Regel positiv geladene radikalische Analytmoleküle entstehen. Die Elektronen haben in der Regel eine Energie von 70eV. Durch die Bildung von Radikalkationen in der Gasphase kommt es je nach chemischer Struktur zu einer Reihe unimolekularer Zerfallsreaktionen, die charakteristische Fragmentsignale erzeugen. Es kommt auch vor, dass das eigentliche Molekülionensignal überhaupt nicht zu sehen ist. Voraussetzung für eine EI-Ionisierung ist, dass die Probe unzersetzt im Hochvakuum verdampfbar ist. Geeignete Beispielstrukturen sind:
Inhalt ausklappen Inhalt einklappen CI (Chemical Ionization)
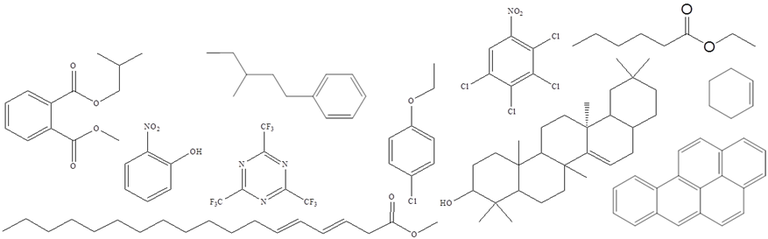
Bei der Chemischen Ionisation wird in die Ionenquelle zu den thermisch verdampften Probenmolekülen ein Überschuß an Reaktandgas eingelassen, das durch Elektronenbeschuss (150 eV) ionisiert wird. Die durch den Elektronenbeschuss gebildeten Primärionen des Reaktandgases reagieren durch eine Serie von Stößen mit weiteren Reaktandgasmolekülen zu den eigentlich ionisierend wirkenden stabilen Ionen (CI-Plasmaionen). Diese Reaktandgasionen sind Brönsted-Säuren. Sie ionisieren Analyt-Moleküle in der Gasphase durch Protonierung in Ionen-Molekül-Reaktionen. In der Regel sind CI-Spektren deutlich fragmentärmer als entsprechende EI-Spektren und zeigen höhere relative Molekülionenintensitäten. Geeignete Beispielstrukturen sind:
Inhalt ausklappen Inhalt einklappen FD/FI/LIFDI (Field Desorption)APCI (Atmospheric pressure chemical ionization)
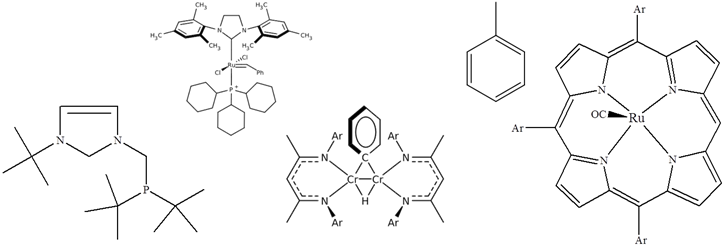
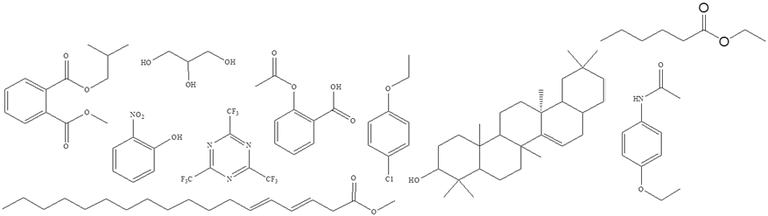
Bei der Feldionisation werden Moleküle in einem elektrischen Feld mit einer hohen Feldstärke ionisiert. Diese lassen sich erreichen, indem die Anode aus einem Metalldraht mit zahlreichen Spitzen (Mikronadeln aus Graphitdentriten) versehen ist. Zwischen der Anode und der Kathode als Gegenelektrode liegt eine Spannung von einigen tausend Volt an. Die Probe wird im gasförmigen Zustand zugeführt (FI) oder ein gelöster oder flüssiger Analyt wird vorher auf der Emitteroberfläche (Anode) adsorbiert (FD). Die Ionisation findet sowohl im Raum zwischen den Elektroden als auch an der Oberfläche der Anode statt. Bei dieser Methode werden die Moleküle nur wenig fragmentiert. Wegen der schonenden Ionisierung eignet sich diese Methode zur Analyse schwer flüchtiger oder thermisch labiler Substanzen. Bei der LIFDI wird durch den Druckunterschied zwischen Normaldruck und Vakuum ein flüssiger Analyt über eine Kapillare direkt auf den Graphitdendriten gespritzt. Diese Methode ist speziell für das Analysieren von luft- und wasserempfindlichen Substanzen geeignet. Geeignete Beispielstrukturen sind:
Elektronenmikroskopische Aufnahme von FD-Emitter-FädenBei der APCI findet eine Primärionisation von Luftmolekülen im Lichtbogen statt. Die Luft-Primärionen übertragen in der Gasphase Ladungen (in Form von Protonen) auf die Analytmoleküle oder abstrahieren sie - je nach Polarität. Die Methode ist wie die ESI sehr schonend und es kommt normalerweise zu keinen Fragmentierungen. Die APCI eignet sich für Moleküle mit nur wenigen Heteroatomen, die mit ESI nicht effizient ionisiert werden können. Es MÜSSEN aber wie bei ESI protonierbare oder deprotonierbare Heteroatome vorhanden sein! Ein großer Unterschied zur ESI besteht darin, dass bei der APCI nur einfach geladene Analyt-Ionen entstehen. Unter anderem weil die meisten Analysatortypen in ihrem messbaren m/z-Bereich beschränkt sind, eignet sich APCI nur für Verbindungen bis ca. 1.5 kDa. Hinsichtlich verwendbarer Lösungsmittel ist APCI toleranter als ESI. Am gebräuchlichsten sind wie bei ESI Methanol und Acetonitril. Gut verwendbar sind aber auch Ethanol, Propanol, Isopropanol, Butanol, Aceton, Chloroform, Toluol, Dichlormethan, Wasser und Kohlenwasserstoffe (wie z.B. Pentan, Hexan, Cyclohexan, etc.). Geeignete Beispielstrukturen sind:
Inhalt ausklappen Inhalt einklappen ASAP (Atmospheric pressure Solids Analysis Probe)
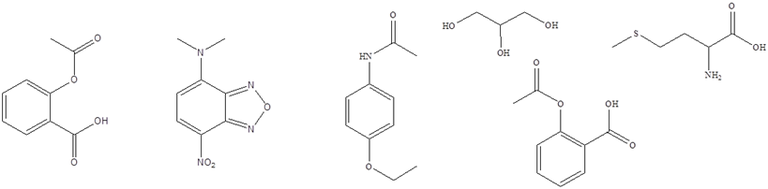
ASAP ist eine etwas exotischere Ionisierungsmethode, die für spezielle Anwendungen geeignet ist. Wir bieten sie derzeit nicht in der Routine, aber auf Nachfrage an. Durch das Einführen eines mit Analytmolekülen belegten Schmelzpunktröhrchens (Sonde) in einem heißen Stickstoffstrom wird der Feststoff von der Oberfläche des Röhrchens verdampft und anschließend durch die Koronaentladung einer APCI-Quelle bei Atmosphärendruck ionisiert. Der heiße Gasstrom (350-500°C) wird entweder vom APCI- oder von einem ESI-Zerstäuber bereitgestellt. Die Quelle kommt somit komplett ohne Lösungsmittel aus. Geeignete Beispielstrukturen sind:
Inhalt ausklappen Inhalt einklappen ESI (Electrospray-Ionization)
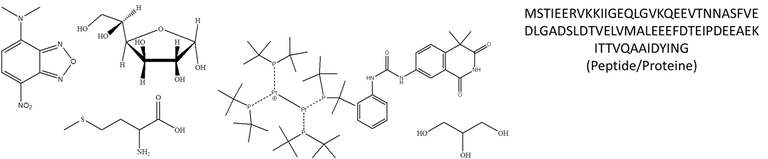
Bei der ESI wird der Analyt gelöst in einem Lösungsmittelgemisch durch eine Kapillare versprüht, an der eine Hochspannung von bis zu 5 kV anliegt. Je nach Polarität der Spannung und der chemischen Eigenschaften des Analyten findet in der Regel eine Protonenaufnahme oder -abgabe statt. Die feinen Tröpfchen des Sprays verlieren auf ihrem Weg von der Spray-Kapillare bis zur Einlasskapillare des Massenspektrometers beständig Lösungsmittelmoleküle. Die Ladungsdichte nimmt zu, was zur Abstoßung der einzelnen Ladungen untereinander führt. Wenn die Ladungsdichte durch Verdunstung hoch genug ist, kommt es zur sogenannten Coulomb-Explosion. Mit ESI werden je nach Masse mehrere Ladungen auf die Analytmoleküle übertragen. Als Faustregel gilt, dass pro 1000 Da ca. 1 Ladung übertragen wird. Da alle MS-Analysatoren nach dem m/z trennen, kann man mit allen Analysatortypen auch sehr große Moleküle (100 kDa und mehr) mit ESI-MS unter Verwendung nahezu jeden Analysators messen. Die Signale liegen im m/z-Spektrum in der Regel immer unterhalb 2000 m/z! Für ESI gut geeignete Lösungsmittel sind Wasser (meist mit Zusatzstoffen wie z.B. Ameisensäure), Methanol, Acetonitril, Ethanol, Isopropanol. Um die Protonierung bzw. Deprotonierung zu beeinflussen eigenen sich Zusätze wie org. Säuren (Ameisensäure) oder Essigsäure. Trifluoressigsäure ist aufgrund ihrer ionensuppressiven Eigenschaften nur bedingt geeignet, aber möglich. Weniger gebräuchlich sind Aceton, Tetrahydrofuran und Formamid. Ausschließlich mit Zusätzen verwendbar wie z.B. Ameisensäure sind Dichlormethan, Chloroform, Toluol, Hexan und andere Kohlenwasserstoffe (Pentan, Cyclohexan, etc.).
Für eine erfolgreiche Ionisierung mittels ESI müssen protonierbare oder deprotonierbare Heteroatome vorhanden sein! Geeignete Beispielstrukturen sind:
Inhalt ausklappen Inhalt einklappen MALDI (Matrix Assisted Laser Desorption Ionization)
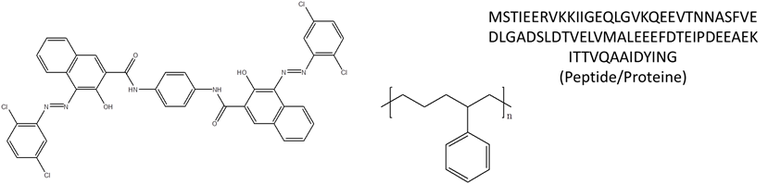
Bei der MALDI wird der Analyt in gelöster Form mit einer Matrixlösung auf einem Target vermischt und zur Kristallisation gebracht. Dieses Target wird dann ins Hochvakuum eines MALDI-TOFs überführt und mit kurzen Laserimpulsen beschossen. Dabei verdampft lokal Matrix und reißt Analytmoleküle mit ins Hochvakuum des Massenspektrometers. Bei diesem Prozess kommt es zu einer Ladungsübertragung. Die sich nun in der Gasphase befindlichen Ionen werden in einem elektrischen Feld beschleunigt und in einer feldfreien Driftstrecke ihrem m/z-Verhältnis nach aufgetrennt. MALDI führt überwiegend zur Bildung einfach-geladener Molekülionen. Fragmentionen werden in der Regel nicht beobachtet, obwohl die gebildeten Ionen metastabil sind und während ihrem "Flug" durch das Hochvakuum der feldfreien Driftstrecke zerfallen. Geeignete Beispielstrukturen sind genrell größere Moleküle, bis hin zu Makromolekülen: